《分子診斷檢驗程序性能驗證指南》深度解讀 引領精準醫療時代的技術研發與質控新標準
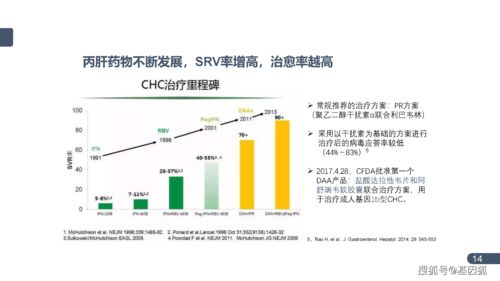
在精準醫療與個體化治療日益成為主流的今天,分子診斷技術以其高特異性、高靈敏度的優勢,已成為疾病診斷、預后評估及用藥指導的核心工具。技術的飛速發展必然伴隨對檢驗結果準確性、可靠性與可比性的嚴苛要求。因此,對分子診斷檢驗程序進行系統、科學的性能驗證,是確保其臨床應用價值與安全性的基石。近期發布的《分子診斷檢驗程序性能驗證指南》(以下簡稱《指南》)為這一關鍵環節提供了權威的技術框架與實踐路徑,對診斷技術的研發與轉化具有深遠的指導意義。
一、《指南》的核心目標與適用范圍
《指南》的核心目標在于規范分子診斷檢驗程序(包括實驗室自建方法及商品化試劑盒)在臨床正式應用前的性能確認活動。它適用于所有基于核酸(DNA/RNA)檢測的定性、定量及分型項目,如病原體檢測、遺傳病診斷、腫瘤伴隨診斷、藥物基因組學等。其根本宗旨是確保任何新建立或重大修改的檢驗程序,其性能指標能夠滿足臨床預期用途的需求,為患者管理和醫學決策提供可靠依據。
二、性能驗證的關鍵指標解讀
《指南》系統闡述了對分子診斷程序進行驗證時必須評估的核心性能參數,為技術研發設定了明確的“質量靶點”:
- 分析靈敏度(檢測限): 這是驗證的起點與重點。對于定性檢測,需確定能穩定檢出目標核酸的最低濃度(95%檢出率);對于定量檢測,則需確定定量下限。研發過程中,必須使用經標定的標準品或臨床樣本梯度稀釋系列,進行多次重復試驗,以科學數據界定方法的檢測能力邊界。
- 分析特異性: 包括交叉反應性與干擾性。《指南》強調需驗證方法與相近物種病原體、同源基因序列、常見內源性及外源性物質(如血紅蛋白、免疫球蛋白、常用藥物等)的交叉反應情況。高特異性是避免假陽性的關鍵,尤其在多重檢測或復雜背景樣本中至關重要。
- 精密度(重復性與再現性): 反映方法在相同或不同條件下的結果一致性。需評估日內、日間以及不同操作者、不同儀器、不同試劑批號間的變異。《指南》建議使用至少兩個濃度水平(包含臨界值附近)的樣本進行多天多次重復檢測,通過標準差或變異系數來量化精密度,這是評估方法穩定性和可靠性的核心。
- 準確度/正確度: 評價檢測結果與真值或參考方法的一致性。可通過與公認的參考方法比較、檢測有證標準物質、或進行臨床樣本的回收試驗等方式進行。對于腫瘤基因突變等復雜檢測,采用經過嚴格驗證的參考樣本或參加權威能力驗證是重要手段。
- 可報告范圍(定量線性): 對于定量項目,必須驗證方法在聲稱的濃度范圍內,其檢測結果與真實濃度呈線性關系的區間,并確定線性回歸方程的相關參數。
- 參考區間/臨床決定限: 根據檢測項目的臨床意義,通過大樣本的健康人群或特定疾病人群研究,建立或驗證結果的解釋區間或臨界值。
三、對診斷技術研發的指導意義與挑戰
《指南》不僅是一份質量控制文件,更為診斷技術的全周期研發注入了“性能優先”的理念:
- 研發初期即植入驗證思維: 技術原理設計、引物探針篩選、反應體系優化時,就必須前瞻性地考慮如何滿足上述性能參數的驗證要求。例如,在開發CRISPR或數字PCR等前沿技術時,需同步設計驗證其超高靈敏度與特異性的方案。
- 推動標準化與參考物質體系構建: 《指南》對準確度驗證的強調,將倒逼行業加速開發適用于不同檢測靶標(尤其罕見突變、融合基因等)的、可溯源的參考物質與標準品,這是提升行業整體可比性的基礎。
- 加速實驗室自建方法的規范化與轉化: 對于針對罕見病或前沿靶點的LDTs,《指南》提供了清晰的驗證路線圖,有助于其從科研向臨床安全、合規地轉化,填補市場空白。
- 應對復雜樣本與集成系統的挑戰: 隨著液體活檢、多組學聯檢、POCT一體化設備等新技術形態的出現,性能驗證面臨樣本基質復雜、多指標互擾、系統集成度高等新挑戰。《指南》的原則性要求促使研發者必須針對這些新場景設計更嚴謹、更具創新性的驗證方案。
四、
《分子診斷檢驗程序性能驗證指南》的出臺與解讀,標志著我國分子診斷行業正從快速發展期邁向高質量、規范化發展的新階段。它如同一把精準的標尺,為診斷技術的研發者劃定了從技術創新到臨床可信的必由之路。技術研發與性能驗證必將更深度地融合:以臨床需求為導向,以驗證標準為基準,推動更多精準、可靠、可及的分子診斷產品問世,最終惠及廣大患者,夯實精準醫療的基石。
如若轉載,請注明出處:http://m.tiantiancha.org.cn/product/72.html
更新時間:2026-02-27 17:34:26